ATOM NEDİR?
Maddenin yapı taşına atom denir. Atom çerisinde de daha küçük parçacıklar bulunmaktadır. Atom içerisinde proton, nötron ve elektron bulunur.
Proton ve nötron atomun çekirdeğinde, elektron ise çekirdeğin etrafında hareket etmektedir.
Elektronlar çok geniş bir alanda bulunmaktadırlar.
Bir atomu futbol sahası kadar büyüttüğümüzde çekirdek başlama noktasında bulunan bir böcek kadar olsa, elektronların bulundukları hacim futbol sahası kadardır.
Proton: Çekirdekte bulunur. Yükü + dır.
Nötron: Kütlesi protonun kütlesine eşittir. Çekirdekte bulunur. Yüksüzdür(Nötr).
Elektron: Kütlesi protonun 1/200 kadardır. Çekirdek etrafında çok hızlı hareket eder. Yükü (-) dir.
- Aynı cins her atomun nötron ve elektron sayıları farklı olabilir. Elektronlar alınıp verilebilir, nötron sayıları da değişebilmektedir.
- Bir atomun kimliğini protonlar belirler. Aynı cins atomların proton sayıları da aynıdır.
Atom iki kısımdan oluşur :
1-Çekirdek (merkez) ve 2-Katmanlar (yörünge; enerji düzeyi)
Çekirdek, hacim olarak küçük olmasına karşın, atomun tüm kütlesini oluşturur. Çekirdekte proton ve nötronlar bulunur. Elektronlar ise çekirdek çevresindeki katmanlarda bulunur.
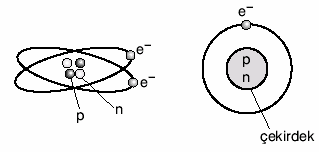
Elektronların çekirdek etrafında dönme hızı, 2,18.108 cm/sn’dir.
Elementlerin Çekirdekte bulunan protonlar, atomun ( o elementin) tüm kimyasal ve fiziksel özelliklerini belirler.
Proton sayısı atomlar (elementler) için ayırt edici özelliktir. Yani proton sayısının farklı olması elementin diğerinden farklı olduğu anlamına gelir.
Elektronların bulunma olasılığının olduğu bölgelere elektron bulutu denir.
Kimyasal olaylarda (reaksiyonlarda) yalnızca elektron sayısı değişir. Proton ve nötron, çekirdekte bulunduğu için sayıları değişmez.
Atomun Yapısı
 Maddeleri oluşturan taneciklerin tümü hareketli taneciklerdir. Yemek tuzunu su içerisine attığımızda çözünerek suyun her tarafına yayılması, odaya sıkılan bir parfümün odanın her yerine yayılması gibi özellikler bu durumu göstermektedir. Ancak elektrik akımını iletmeyen katı hâldeki yemek tuzunun, suda çözündüğünde oluşan karışımın elektrik akımını iletir hâle gelmesi, plâstik bir tarağın yün kazağa sürtülmesi sonucunda küçük kağıt parçalarını çekebilmesi maddeyi oluşturan temel parçacıklar olan atomların aslında daha da küçük taneciklerden oluştuğu ve bir kısım olaylar sonucunda da bu tanecikler arası etkileşimlerin ve değişimlerin olduğu sonucunu ortaya çıkarmaktadır.
Maddeleri oluşturan taneciklerin tümü hareketli taneciklerdir. Yemek tuzunu su içerisine attığımızda çözünerek suyun her tarafına yayılması, odaya sıkılan bir parfümün odanın her yerine yayılması gibi özellikler bu durumu göstermektedir. Ancak elektrik akımını iletmeyen katı hâldeki yemek tuzunun, suda çözündüğünde oluşan karışımın elektrik akımını iletir hâle gelmesi, plâstik bir tarağın yün kazağa sürtülmesi sonucunda küçük kağıt parçalarını çekebilmesi maddeyi oluşturan temel parçacıklar olan atomların aslında daha da küçük taneciklerden oluştuğu ve bir kısım olaylar sonucunda da bu tanecikler arası etkileşimlerin ve değişimlerin olduğu sonucunu ortaya çıkarmaktadır.
İşte bir atomu oluşturan daha küçük birimlere alt parçacıklar denir. Bu parçacıklar proton, nötron ve elektrondur. Atomları oluşturan alt parçacıklar atom içerisinde farklı konumlarda yer alırlar. Bir atomun temel yapısı iki ana bölgeden oluşur.
a. Atom Çekirdeği: Proton ve nötronların bulunduğu yoğun ve küçük hacimli bölgedir.
b. Enerji Katmanları: Elektronların dağıldığı, çekirdek hacmine göre oldukça büyük hacimli ve boşlukların çok olduğu bölgedir. Buna göre atomun yapısını tekrar sınıflandırırsak, atom temel olarak iki ana bölgeden meydana gelir. Bunlar da atom çekirdeği ve enerji katmanları (enerji seviyeleri) dir. Daha sonra atom çekirdeğinde ise proton ve nötronlar bulunur. Enerji katmanlarında ise sadece elektronlar yer alır diyebiliriz. Atomu oluşturan alt parçacıkların yükleri birbirinden farklıdır. Protonlar pozitif (+) yüklü, elektronlar negatif (–) yüklü ve nötronlar ise yüksüz parçacıklardır.
Atom çekirdeğinde proton ve nötronlar, çekirdeğin dışındaki katmanlarda ise elektronlar bulunur.

- İzotop Atomlar: Proton sayıları, aynı nötron sayıları farklı olan atomlardır. Bu atomların nötron sayıları farklı olduğundan kütle numaralarıda farklı olur.
- İzotop atom: Bir elementin izotop nötr atomlarının kimyasal özellikleri aynıdır. Fiziksel özellikleri ise farklıdır.
İzotop olan fakat elektron sayıları farklı olan taneciklerin ise fiziksel ve kimyasal özellikleri farklıdır. - İzoton Atomlar: Proton sayıları farklı, nötron sayıları aynı olan elementlerdir. Bu atomların hem kimyasal, hem de fiziksel özellikleri farklıdır.
- İzobar Atomlar: Proton sayıları farklı, kütle numaraları (nükleon sayıları) aynı olan elementlerdir. Bu atomların hem kimyasal hem de fiziksel özellikleri farklıdır.
- Allotrop Atomlar: Bir elementin özdeş atomlarının farklı sayı ve dizilişteki şekilleridir. Bu atomlar aynı elemente ait olduğu için kimyasal özellikleri aynıdır. Atomlar farklı sayı ve dizilişte olduğundan fiziksel özellikleri farklı olur.
Atomu oluşturan tanecikler
Atomlar çekirdek ve yörüngelerden oluşmuşlardır. Çekirdekte proton ve nötronlar; yörüngelerde de, elektronlar bulunur.
 PROTON: Atomun çekirdeğinde bulunan, + yüklü taneciklere denir.
PROTON: Atomun çekirdeğinde bulunan, + yüklü taneciklere denir.
Protonun Özellikleri:
- Atomun çekirdeğinde bulunurlar.
- + yüklü taneciklerdir. (Atomun çekirdek yükünü belirler. ) ( Ps=Çy )
- Atomun cinsini belirler. (Ps=An)
- Nötr atomlarda, elektron sayısına eşittir. (Ps=An=Çy=Es)
- Atomun kütlesine etki ederler.
NÖTRON: Atomun çekirdeğinde bulunan yüksüz taneciklere denir.
Nötronun Özellikleri:
- Atomun çekirdeğinde bulunurlar.
- Yüksüz taneciklerdir. (Atomun çekirdek yüküne etki etmezler.)
- Atomun kimyasal özelliklerine, etki etmezler.
- Atomun kütlesine etki ederler.
ELEKTRON: Atomun çekirdeğinin etrafında hareket eden yüklü taneciklere denir.
Elektronun Özellikleri:
- Atomun çekirdeğinin etrafında hareket ederler.
- Yüklü taneciklerdir. (Atomun yüküne etki ederler.)
- Bilhassa değerlik elektronları, atomun kimyasal özelliklerine etki eder.
- Nötr atomlarda Ps = Es dır.
- Atomun kütlesine etkileri ihmal edilir.
TARİH BOYUNCA ATOM HAKKINDA GÖRÜŞLER:
1. Democritus (Demokritus)
Yunanlı bir filozoftur. Maddenin taneciklerden oluştuğu fikrini ortaya attı. Bu taneciklere atomos adını verdi. Bu görüşü bilimsel olarak değil varsayım olarak söylemiştir. Democritus’a göre bütün maddelerin atomları aynıdır, atom görülemez ve bölünemez demiştir.
2. John Dalton
Atom hakkında ilk bilimsel açıklamayı yaptı. Dalton’a göre maddenin en küçük yapı birimi atomdur. Atomların içleri dolu berk kürelerden oluşmaktadırlar. Bütün maddelerin farklı cins atomlardan oluştuğunu da söylemiştir.
3. J.J. Thomson
Atomu üzümlü keke benzettiği modelle açıkladı. Atomun dış katmanı pozitif (+) içinde ise negatif (-) yükler bulunmaktadır. Negatif yüklerin hareket etmediğini söylemiştir. Atomun parçalanabileceğini belirtmiştir.
4. Rutherford
Pozitif yüklere proton adını vermiştir. Protonun bulunduğu yeri çekirdek demiştir. Çekirdek etrafında elektronların hareket halinde olduğunu keşfetti. Yaptığı model güneş sistemine benzetmiştir.
5. Niels Bohr
Bohr atom modeline göre elektronlar çekirdek etrafında rastgele dolanmamaktadır. Elektronlar çekirdeğin belirli uzaklıkdaki katmanlarda bulunmaktadır.
6. Modern atom teorisi
Elektronlar çok hızlı hareket ettikleri için, elektronların yerini belirleyemeyiz. Elektronların bulunma ihtimalinin en fazla olduğu yerlere “Elektron Bulutu” denilmektedir.
Elektronların sabit yörüngeleri olduklarından Bohr atom modelinde olduğu gibi katmanlardan bahsetmek zordur. Katman yerine elektron bulutu kullanılmaktadır.
Not: Geçmişten günümüze atom fikrinde birçok değişiklik olmuştur. Atom konusunda herşeyi bildiğimizi söylememiz mümkün değildir. Atom konusunda çalışmalar devam etmektedir.
Diğer dersimizde Atom Modellerini daha detaylı inceleyeceğiz.


Comments
RSS feed for comments to this post